Vắc-xin mRNA của Pfizer cho COVID đã khơi dậy niềm đam mê sử dụng axit ribonucleic (RNA) làm mục tiêu điều trị.Tuy nhiên, nhắm mục tiêu RNA với các phân tử nhỏ là vô cùng khó khăn.
RNA chỉ có bốn khối xây dựng: adenine (A), cytosine (C), guanine (G) và uracil (U) thay thế thymine (T) được tìm thấy trong DNA.Điều này làm cho tính chọn lọc của thuốc trở thành một trở ngại gần như không thể vượt qua.Ngược lại, có 22 axit amin tự nhiên tạo nên protein, điều này giải thích tại sao hầu hết các loại thuốc nhắm mục tiêu protein đều có tính chọn lọc tương đối tốt.
Cấu trúc và chức năng của ARN
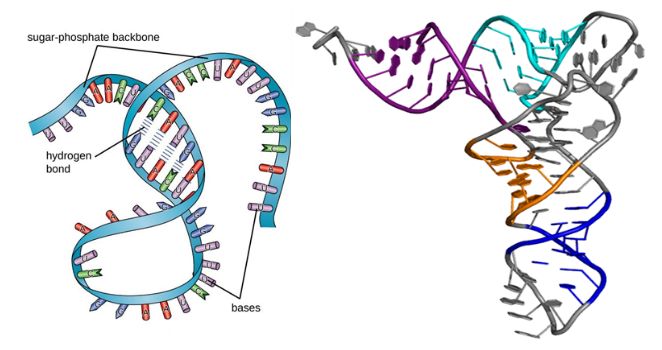
Giống như protein, các phân tử RNA có cấu trúc bậc hai và bậc ba, như thể hiện trong hình bên dưới.Mặc dù chúng là các đại phân tử chuỗi đơn, nhưng cấu trúc thứ cấp của chúng hình thành khi sự ghép đôi bazơ gây ra các chỗ phình ra, các vòng và các vòng xoắn.Sau đó, sự gấp ba chiều dẫn đến cấu trúc bậc ba của RNA, điều cần thiết cho sự ổn định và chức năng của nó.
Hình 1. Cấu trúc của RNA
Có ba loại ARN:
- ARN thông tin (mARN)phiên mã thông tin di truyền từ DNA và được chuyển dưới dạng trình tự cơ sở vào ribosome;tôi
- ARN ribôxôm (rARN)là một phần của các bào quan tổng hợp protein được gọi là ribosome, được xuất ra tế bào chất và giúp dịch thông tin trong mRNA thành protein;
- ARN vận chuyển (tRNA)là liên kết giữa mARN và chuỗi axit amin cấu tạo nên prôtêin.
Nhắm mục tiêu RNA như một mục tiêu điều trị rất hấp dẫn.Người ta đã phát hiện ra rằng chỉ 1,5% bộ gen của chúng ta cuối cùng được dịch thành protein, trong khi 70% -90% được phiên mã thành RNA.Các phân tử RNA là quan trọng nhất đối với tất cả các sinh vật sống.Theo “thuyết trung tâm” của Francis Crick, vai trò quan trọng nhất của RNA là dịch thông tin di truyền từ DNA thành protein.Ngoài ra, các phân tử RNA còn có các chức năng khác, bao gồm:
- Hoạt động như các phân tử bộ chuyển đổi trong quá trình tổng hợp protein;tôi
- Phục vụ như một sứ giả giữa DNA và ribosome;tôi
- Chúng là vật mang thông tin di truyền trong tất cả các tế bào sống;tôi
- Thúc đẩy sự lựa chọn của ribosome đối với các axit amin chính xác, cần thiết để tổng hợp protein mớitrong cơ thể sống.
thuốc kháng sinh
Mặc dù được phát hiện sớm nhất vào những năm 1940, cơ chế hoạt động của nhiều loại kháng sinh vẫn chưa được làm sáng tỏ cho đến cuối những năm 1980.Người ta phát hiện ra rằng một tỷ lệ lớn thuốc kháng sinh hoạt động bằng cách liên kết với các ribosome của vi khuẩn để ngăn chúng tạo ra các protein thích hợp, do đó giết chết vi khuẩn.
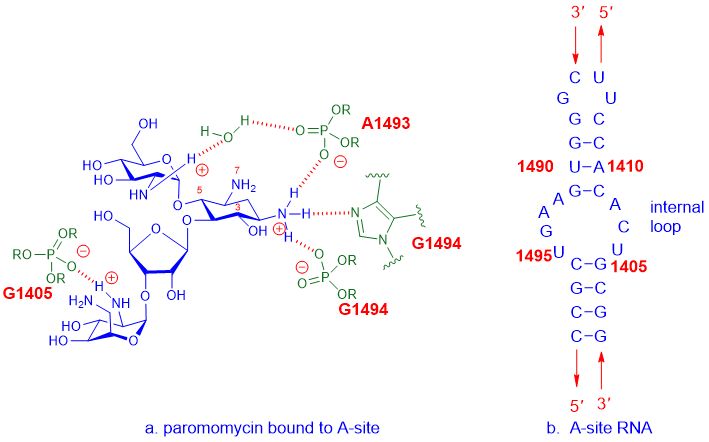
Ví dụ, kháng sinh aminoglycoside liên kết với vị trí A của 16S rRNA, là một phần của tiểu đơn vị 30S ribosome, sau đó can thiệp vào quá trình tổng hợp protein để cản trở sự phát triển của vi khuẩn, cuối cùng dẫn đến chết tế bào.Vị trí A đề cập đến vị trí aminoacyl, còn được gọi là vị trí chấp nhận tRNA.Sự tương tác chi tiết giữa các loại thuốc aminoglycoside, chẳng hạn nhưparomomycin, và trang web A củaE coliRNA được hiển thị dưới đây.
Hình 2. Sự tương tác giữa paromomycin và vị trí A củaE coliARN
Thật không may, nhiều chất ức chế tại chỗ A, bao gồm cả thuốc aminoglycoside, có các vấn đề về an toàn như độc tính trên thận, phụ thuộc vào liều lượng và độc tính trên tai không hồi phục cụ thể.Những độc tính này là kết quả của việc thiếu tính chọn lọc trong các thuốc aminoglycoside để nhận ra các phân tử nhỏ RNA.
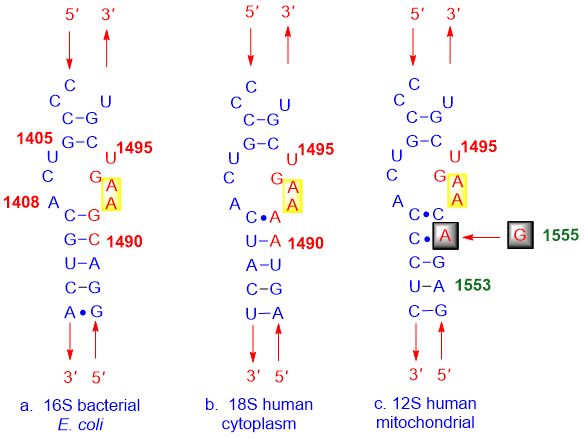
Như thể hiện trong hình bên dưới: (a) cấu trúc của vi khuẩn, (b) màng tế bào người và (c) vị trí A trong ty thể của con người rất giống nhau, làm cho chất ức chế vị trí A liên kết với tất cả chúng.
Hình 3. Liên kết chất ức chế vị trí A không chọn lọc
Kháng sinh Tetracycline cũng ức chế vị trí A của rRNA.Chúng ức chế chọn lọc quá trình tổng hợp protein của vi khuẩn bằng cách liên kết thuận nghịch với vùng xoắn ốc (H34) trên tiểu đơn vị 30S được tạo phức với Mg2+.
Mặt khác, kháng sinh macrolide liên kết gần vị trí thoát (E-site) của đường hầm ribosome của vi khuẩn đối với các peptide mới sinh (NPET) và ngăn chặn một phần nó, do đó ức chế quá trình tổng hợp protein của vi khuẩn.Cuối cùng, kháng sinh oxazolidinone nhưlinezolid(Zyvox) liên kết với một khe hở sâu trong tiểu đơn vị 50S ribosome của vi khuẩn, được bao quanh bởi các nucleotide 23S rRNA.
Antisense oligonucleotide (ASO)
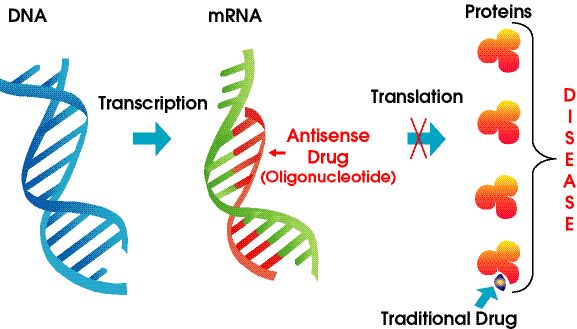
Các loại thuốc antisense là các polyme axit nucleic đã được biến đổi hóa học nhắm vào RNA.Chúng dựa vào cặp bazơ Watson-Crick để liên kết với mARN mục tiêu, dẫn đến làm im lặng gen, phong tỏa không gian hoặc thay đổi mối nối.ASO có thể tương tác với các pre-RNA trong nhân tế bào và các mRNA trưởng thành trong tế bào chất.Chúng có thể nhắm mục tiêu vào các exon, intron và các vùng chưa được dịch mã (UTR).Cho đến nay, hơn một chục loại thuốc ASO đã được FDA chấp thuận.
Hình 4. Công nghệ Antisense
Thuốc phân tử nhỏ nhắm mục tiêu RNA
Vào năm 2015, Novartis đã báo cáo rằng họ đã phát hiện ra một bộ điều chỉnh nối SMN2 có tên là Branaplam, giúp tăng cường sự liên kết của U1-pre-mRNA và giải cứu những con chuột SMA.
Mặt khác, PTC/Roche's Risdiplam (Evrysdi) đã được FDA chấp thuận vào năm 2020 để điều trị SMA.Giống như Branaplam, Risdiplam cũng hoạt động bằng cách điều chỉnh sự ghép nối của các gen SMN2 có liên quan để tạo ra các protein SMN chức năng.
chất làm suy giảm RNA
RBM là viết tắt của RNA-binding motif protein.Về cơ bản, indole sulfonamide là một chất kết dính phân tử.Nó tuyển chọn có chọn lọc RBM39 vào ligase CRL4-DCAF15 E3 ubiquitin, thúc đẩy quá trình đa bào hóa RBM39 và thoái hóa protein.Sự suy giảm di truyền hoặc suy thoái RBM39 qua trung gian sulfonamide gây ra những bất thường đáng kể trong quá trình ghép nối trên toàn bộ bộ gen, cuối cùng dẫn đến chết tế bào.
RNA-PROTAC được phát triển để làm suy giảm các protein gắn RNA (RBP).PROTAC sử dụng trình liên kết để kết nối phối tử ligase E3 với phối tử RNA, phối tử này liên kết với RNA và RBP.Do RBP chứa các miền cấu trúc có thể liên kết với các trình tự oligonucleotide cụ thể, nên RNA-PROTAC sử dụng trình tự oligonucleotide làm phối tử cho protein quan tâm (POI).Kết quả cuối cùng là sự xuống cấp của RBPs.
Gần đây, Giáo sư Matthew Disney của Viện Hải dương học Scripps đã phát minh ra RNAkhảm nhắm mục tiêu ribonuclease (RiboTAC).RiboTAC là một phân tử dị chức năng kết nối phối tử RNase L và phối tử RNA với trình tự liên kết.Nó có thể đặc biệt tuyển dụng RNase L nội sinh cho các mục tiêu RNA cụ thể, sau đó loại bỏ thành công RNA bằng cơ chế phân hủy axit nucleic của tế bào (RNase L).
Khi các nhà nghiên cứu tìm hiểu thêm về sự tương tác giữa các phân tử nhỏ và mục tiêu RNA, nhiều loại thuốc sử dụng phương pháp này sẽ xuất hiện trong tương lai.
Thời gian đăng: 02-08-2023