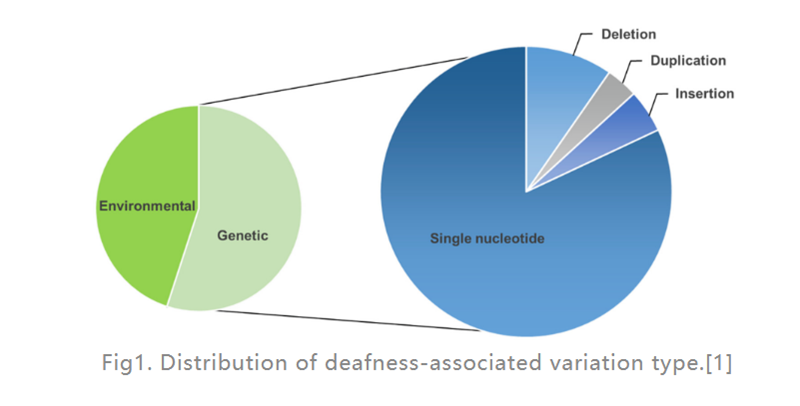
Mất thính giác (HL) là bệnh khuyết tật giác quan phổ biến nhất ở người.Ở các nước phát triển, khoảng 80% trường hợp điếc bẩm sinh ở trẻ em là do yếu tố di truyền.Phổ biến nhất là các khiếm khuyết đơn gen (như trong Hình 1), 124 đột biến gen đã được phát hiện có liên quan đến mất thính giác không đặc hiệu ở người, phần còn lại là do các yếu tố môi trường.Cấy ghép ốc tai điện tử (một thiết bị điện tử được đặt ở tai trong cung cấp kích thích điện trực tiếp đến dây thần kinh thính giác) cho đến nay là lựa chọn hiệu quả nhất để điều trị HL nặng, trong khi máy trợ thính (một thiết bị điện tử bên ngoài giúp chuyển đổi và khuếch đại sóng âm thanh) có thể giúp Bệnh nhân bị HL mức độ trung bình.Tuy nhiên, hiện tại không có loại thuốc nào có thể điều trị bệnh HL di truyền (GHL).Trong những năm gần đây, liệu pháp gen ngày càng được chú ý như một phương pháp đầy hứa hẹn để điều trị rối loạn chức năng tai trong.
Hình1.Phân bố loại biến thể liên quan đến điếc.[1]
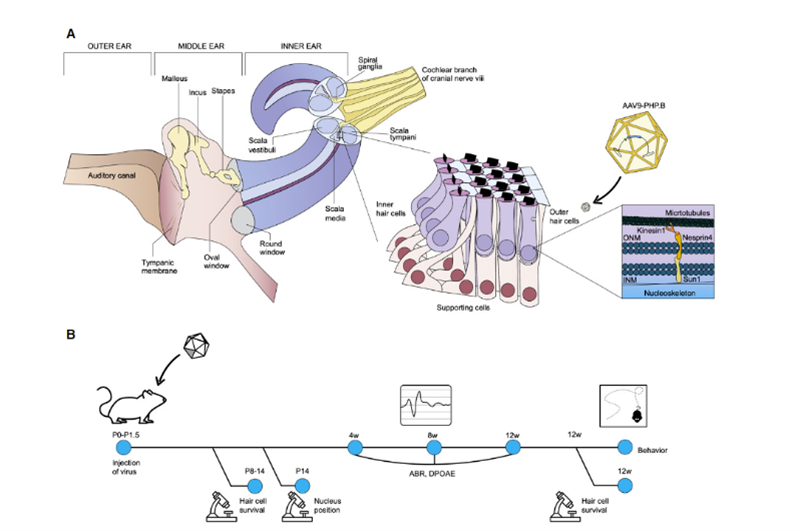
Gần đây, các nhà khoa học từ Viện Salk và Đại học Sheffield đã công bố kết quả nghiên cứu trong Liệu pháp phân tử – Phương pháp & Phát triển lâm sàng [2], cho thấy triển vọng ứng dụng rộng rãi của liệu pháp gen in vivo đối với bệnh điếc di truyền.Uri Manor, trợ lý giáo sư nghiên cứu tại Viện Salk kiêm giám đốc Trung tâm Quang tử sinh học tiên tiến Waitt, cho biết ông sinh ra đã bị mất thính lực nghiêm trọng và cảm thấy rằng việc phục hồi thính giác sẽ là một món quà tuyệt vời.Nghiên cứu trước đây của ông đã phát hiện ra rằng Eps8 là một protein điều hòa actin với các hoạt động liên kết và đóng nắp actin;trong các tế bào lông ốc tai, phức hợp protein được hình thành bởi Eps8 với MYO15A, WHIRLIN, GPSM2 và GNAI3 chủ yếu tồn tại ở hầu hết các đầu của sợi lông tơ dài, cùng với MYO15A định vị BAIAP2L2 ở đầu sợi lông tơ ngắn hơn, được yêu cầu để duy trì các bó tóc.Do đó, Eps8 có thể điều chỉnh độ dài của lông mao lập thể của các tế bào lông, điều này rất cần thiết cho chức năng nghe bình thường;Việc xóa hoặc đột biến Eps8 sẽ dẫn đến lông mao lập thể ngắn, khiến nó không thể chuyển đổi âm thanh thành tín hiệu điện một cách chính xác để não bộ nhận thức, từ đó dẫn đến điếc..Đồng thời, cộng tác viên Walter Marcotti, giáo sư tại Đại học Sheffield, phát hiện ra rằng các tế bào tóc không thể phát triển bình thường nếu không có Eps8.Trong nghiên cứu này, Manor và Marcotti đã hợp tác để điều tra xem liệu việc thêm Eps8 vào các tế bào lông mao lập thể có thể khôi phục chức năng của chúng và từ đó cải thiện khả năng nghe ở chuột hay không.Nhóm nghiên cứu đã sử dụng vectơ Anc80L65 của vi-rút liên quan đến adeno (AAV) để đưa trình tự mã hóa chứa EPS8 loại hoang dã vào ốc tai của chuột Eps8-/- P1-P2 sơ sinh bằng cách tiêm màng cửa sổ tròn;trong các tế bào lông ốc tai của chuột Chức năng của lông mao đã được sửa chữa trước khi chúng trưởng thành;và hiệu ứng sửa chữa được đặc trưng bởi công nghệ hình ảnh và phép đo stereocilia.Kết quả cho thấy Eps8 làm tăng độ dài của lông mao và phục hồi chức năng của tế bào lông ở các tế bào tần số thấp.Họ cũng phát hiện ra rằng, theo thời gian, các tế bào dường như mất khả năng được giải cứu bằng liệu pháp gen này.Hàm ý là phương pháp điều trị này có thể cần được thực hiện trong tử cung, vì các tế bào lông Eps8-/- có thể đã trưởng thành hoặc tích lũy tổn thương không thể sửa chữa sau khi chuột được sinh ra.“Eps8 là một loại protein có nhiều chức năng khác nhau và vẫn còn rất nhiều điều cần khám phá,” Manor nói.Nghiên cứu trong tương lai sẽ bao gồm điều tra tác dụng của liệu pháp gen Eps8 trong việc khôi phục thính giác ở các giai đoạn phát triển khác nhau và liệu có thể kéo dài cơ hội điều trị hay không.Thật trùng hợp, vào tháng 11 năm 2020, Giáo sư KarenB Avraham của Đại học Tel Aviv ở Israel đã công bố kết quả của mình trên tạp chí EMBO Molecular Medicine [3], sử dụng công nghệ liệu pháp gen cải tiến để tạo ra vi rút tổng hợp vô hại liên quan đến adeno AAV9-PHP.B, Khiếm khuyết gen trong tế bào lông của chuột Syne4-/- đã được sửa chữa bằng cách tiêm một loại vi-rút mang trình tự mã hóa của Syne4 vào tai trong của chuột, cho phép nó xâm nhập vào tế bào lông và giải phóng vật liệu di truyền mang theo, cho phép chúng trưởng thành và hoạt động bình thường (như trong Hình 2).
Hình2.Sơ đồ giải phẫu tai trong, tập trung vào cơ quan Corti và chức năng tế bào của nesprin-4.
Có thể thấy, việc sử dụng liệu pháp gen nhằm đạt mục đích điều trị các bệnh di truyền ở cấp độ gen bằng cách đưa vào, loại bỏ hoặc sửa chữa bất kỳ gen đột biến nào để điều trị (tức là kiểm soát sự biến đổi gen của bệnh) mang lại hiệu quả lâm sàng cao.triển vọng ứng dụng.Các phương pháp trị liệu gen hiện tại đối với bệnh điếc do thiếu gen có thể được chia thành các loại sau:
thay thế gen
Thay thế gen được cho là hình thức trị liệu gen “đơn giản” nhất, dựa trên việc xác định và thay thế một gen khiếm khuyết bằng một bản sao gen bình thường hoặc kiểu hoang dã.Nghiên cứu liệu pháp gen tai trong thành công đầu tiên đối với chứng mất thính giác do xóa gen vận chuyển glutamate dạng túi 3 (VGLUT3);Việc cung cấp biểu hiện quá mức VGLUT3 ngoại sinh qua trung gian AAV1 trong các tế bào lông tai trong (IHC) Có thể dẫn đến phục hồi thính giác bền vững, phục hồi hình thái khớp thần kinh dải một phần và phản ứng co giật [4].Tuy nhiên, trong các ví dụ bao gồm hai thay thế gen do AAV được mô tả trong phần giới thiệu ở trên, điều quan trọng cần lưu ý là các mô hình chuột được sử dụng cho một số loại rối loạn mất thính giác di truyền do xóa gen nhất định khác với con người về mặt thời gian và ở chuột P1 , tai trong đang trong giai đoạn phát triển trưởng thành.Ngược lại, con người được sinh ra với một tai trong trưởng thành.Sự khác biệt này ngăn cản khả năng áp dụng kết quả của chuột để điều trị chứng rối loạn điếc di truyền ở người trừ khi liệu pháp gen được chuyển giao cho tai chuột trưởng thành.
Chỉnh sửa gen: CRISPR/Cas9
So với “thay thế gen”, sự phát triển của công nghệ chỉnh sửa gen đã mở ra bình minh cho việc điều trị tận gốc các bệnh di truyền.Điều quan trọng là phương pháp chỉnh sửa gen đã bù đắp được những thiếu sót của phương pháp trị liệu gen biểu hiện quá mức truyền thống không phù hợp với các bệnh điếc di truyền trội và vấn đề phương pháp biểu hiện quá mức không tồn tại được lâu.Sau khi các nhà nghiên cứu Trung Quốc loại bỏ cụ thể alen đột biến Myo6C442Y ở chuột Myo6WT/C442Y bằng hệ thống chỉnh sửa gen AAV-SaCas9-KKH-Myo6-g2, và trong vòng 5 tháng sau khi loại bỏ, chức năng thính giác của mô hình chuột đã được khôi phục;đồng thời, người ta cũng nhận thấy rằng tỷ lệ sống sót của các tế bào lông ở tai trong được cải thiện, hình dạng của lông mao trở nên đều đặn và các chỉ số điện sinh lý được điều chỉnh [5].Đây là nghiên cứu đầu tiên trên thế giới sử dụng công nghệ CRISPR/Cas9 trong điều trị bệnh điếc di truyền do đột biến gen Myo6 và là một tiến bộ nghiên cứu quan trọng của công nghệ chỉnh sửa gen trong điều trị bệnh điếc di truyền.Bản dịch lâm sàng của điều trị cung cấp một cơ sở khoa học vững chắc.
Phương pháp cung cấp liệu pháp gen
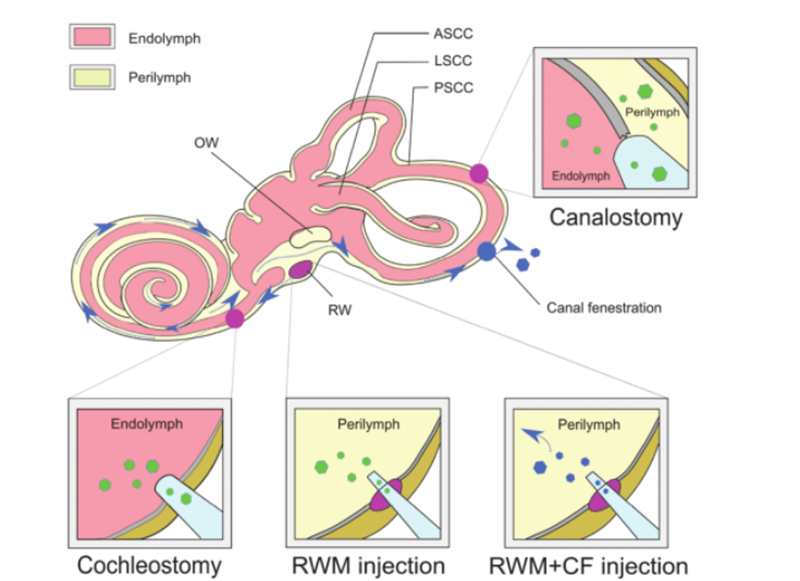
Để liệu pháp gen thành công, các phân tử DNA trần không thể thâm nhập vào tế bào một cách hiệu quả do tính ưa nước và điện tích âm của các nhóm phốt phát và để đảm bảo tính toàn vẹn của các phân tử axit nucleic được bổ sung, phải chọn một phương pháp an toàn và hiệu quả.DNA bổ sung được chuyển đến tế bào hoặc mô đích.AAV được sử dụng rộng rãi như một phương tiện vận chuyển để điều trị bệnh do tác dụng lây nhiễm cao, khả năng sinh miễn dịch thấp và tính hướng nhiệt rộng đối với các loại mô khác nhau.Hiện tại, một lượng lớn công trình nghiên cứu đã xác định tính hướng của các phân nhóm AAV khác nhau so với các loại tế bào khác nhau trong ốc tai chuột.Sử dụng các đặc điểm phân phối AAV kết hợp với các trình khởi động dành riêng cho tế bào có thể đạt được biểu thức dành riêng cho tế bào, điều này có thể làm giảm các hiệu ứng ngoài mục tiêu.Ngoài ra, để thay thế cho các vectơ AAV truyền thống, các vectơ AAV tổng hợp mới liên tục được phát triển và cho thấy khả năng tải nạp vượt trội ở tai trong, trong đó AAV2/Anc80L65 được sử dụng rộng rãi nhất.Các phương pháp phân phối phi vi-rút có thể được chia thành các phương pháp vật lý (vi tiêm và điện di) và phương pháp hóa học (dựa trên lipid, dựa trên polymer và các hạt nano vàng).Cả hai phương pháp đã được sử dụng trong điều trị rối loạn điếc di truyền và đã cho thấy những ưu điểm và hạn chế khác nhau.Ngoài phương tiện vận chuyển cho liệu pháp gen như một phương tiện, các phương pháp khác nhau để quản lý gen in vivo có thể được sử dụng dựa trên các loại tế bào đích khác nhau, đường dùng và hiệu quả điều trị.Cấu trúc phức tạp của tai trong khiến việc tiếp cận các tế bào mục tiêu trở nên khó khăn và việc phân phối các tác nhân chỉnh sửa bộ gen bị chậm.Mê cung màng nằm trong mê cung xương của xương thái dương và bao gồm ống ốc tai, ống bán nguyệt, utricle và bóng.Sự cô lập tương đối của nó, lưu thông bạch huyết tối thiểu và tách khỏi máu bằng hàng rào mê cung máu hạn chế việc cung cấp phương pháp trị liệu có hệ thống hiệu quả chỉ cho chuột sơ sinh.Để có được các chuẩn độ virus phù hợp với liệu pháp gen, cần tiêm trực tiếp vec tơ virus vào tai trong.Các đường tiêm đã được thiết lập bao gồm [6]: (1) màng cửa sổ tròn (RWM), (2) mở khí quản, (3) mở thông nội dịch hoặc ốc tai quanh ngoại dịch, (4) màng cửa sổ tròn cộng với thông ống (CF) (như trong Hình 3).
Hình 3.Tai trong cung cấp liệu pháp gen.
Mặc dù nhiều tiến bộ đã được thực hiện trong liệu pháp gen, nhưng dựa trên các mục tiêu dịch mã lâm sàng, cần phải thực hiện nhiều công việc hơn trước khi liệu pháp gen có thể trở thành lựa chọn điều trị đầu tay cho bệnh nhân mắc bệnh di truyền, đặc biệt là trong việc phát triển các vectơ và phương pháp phân phối an toàn và hiệu quả.Nhưng chúng tôi tin rằng trong tương lai gần, những phương pháp điều trị này sẽ trở thành một phần chính của liệu pháp cá nhân hóa và sẽ có tác động cực kỳ tích cực đến cuộc sống của những người mắc chứng rối loạn di truyền và gia đình họ.
Foregene cũng đã tung ra một bộ công cụ sàng lọc thông lượng cao cho các gen mục tiêu, nhanh chóng và có thể thực hiện các phản ứng sao chép ngược và qPCR mà không cần chiết xuất RNA.
Liên kết sản phẩm
Cell Direct RT-qPCR kit—Taqman/SYBR GREEN I
Để biết thêm thông tin sản phẩm, vui lòng liên hệ:
Thời gian đăng: 02-09-2022